5月13日,药物临床试验登记与信息公示平台显示,赛诺菲的抗CD40L单抗SAR441344(frexalimab)在中国启动了III期临床试验。该产品于2023年12月首次进入III期阶段。

该研究是一项随机、双盲、安慰剂对照临床试验,拟在国内招募20例受试者,旨在评估SAR441344在非复发性继发进展型多发性硬化成人患者中的安全性和有效性。研究的主要终点为6个月内患者发生经复合指标确认的残疾进展(cCDP)的时间。
SAR441344可阻断适应性免疫细胞(T/B细胞)和先天性免疫细胞(巨噬细胞和树突状细胞)激活并发挥功能必需的CD40/CD40L共刺激通路,同时不会耗竭淋巴细胞,以此达到治疗多发性硬化症的急性和慢性神经炎症目的。该产品的开发进度在CD40L赛道处于第一梯队,有望成为该疾病领域首款CD40L靶向药物。
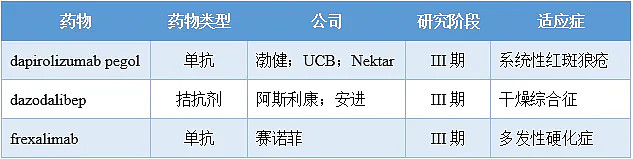
后期在研CD40L靶向药物
在II期研究中,SAR441344可将MS患者的新钆增强T1大脑病灶面积减少89%。若III期研究顺利完成,赛诺菲计划在2025年提交SAR441344用于治疗多发性硬化症的上市申请。
除此之外,赛诺菲也另辟蹊径探索该药物在保护1型糖尿病患者的胰岛β细胞功能上的潜力,似有将其与用于延缓1型糖尿病进展的teplizumab(商品名:Tzield)打组合拳之意。
$赛诺菲-安万特(SNY)$ $Biogen制药(BIIB)$ $阿斯利康(AZN)$
近期医药行业热门研究报告免费下载:
2023年全球药品销售额TOP100网页链接
医药魔方-2019-2023年创新药临床研究报告网页链接
2024年热门企业Q1财报合集网页链接
ASCO 2024 口头报告新闻汇总网页链接
医药BD专题报告/深度文章汇总网页链接
更多相关报告和医药资讯持续更新,请持续关注医药魔方ByDrug 网页链接